肝癌(HCC)的發(fā)病率不斷上升,對(duì)其進(jìn)行特異性診斷和準(zhǔn)確治療具有重要意義�����,但目前面臨著一些挑戰(zhàn)�。例如,18F-FDG PET成像作為腫瘤診斷和定位的金標(biāo)準(zhǔn)����,在HCC中由于其腫瘤內(nèi)攝取低而顯示出局限性,這可能是由于葡萄糖-6-磷酸酶(G6Pase)的去磷酸化作用所致����。G6Pase是一種糖異生酶,在分化良好的HCC中高度表達(dá)�,將葡萄糖-6-磷酸轉(zhuǎn)化為葡萄糖,從而導(dǎo)致18F-FDG在腫瘤細(xì)胞內(nèi)的保留減少�。因此,新的PET探針有望用于HCC成像。
光動(dòng)力療法是一種無創(chuàng)且有前景的癌癥治療方法�����,具有最小的全身毒性和時(shí)空可控性����。在此背景下,研究者認(rèn)為開發(fā)一種用于HCC成像和光動(dòng)力治療的綜合治療劑具有重要意義��。然而��,當(dāng)應(yīng)用于成像和治療時(shí)����,藥物應(yīng)該具有不同的瘤內(nèi)保留。具有合適腫瘤保留時(shí)間的顯像劑���,如放射性核素標(biāo)記的FAPI�����,在用于HCC治療時(shí)總是被認(rèn)為腫瘤保留時(shí)間不足�����。
影像學(xué)檢查后腫瘤滯留時(shí)間過長(zhǎng)���,不僅延長(zhǎng)了護(hù)理時(shí)間�����,而且造成了不必要的放射損傷。然而�,腫瘤治療藥物需要更長(zhǎng)的腫瘤滯留時(shí)間來增強(qiáng)抗腫瘤作用。為了構(gòu)建一種在腫瘤成像和光動(dòng)力治療中同時(shí)滿足腫瘤內(nèi)滯留要求的藥物�,研究者開發(fā)了一種以ASGPR為靶點(diǎn)的乳酸(LA)衍生物,用于肝癌的熒光/ PET雙模成像和光動(dòng)力治療�。
ASGPR是一種c型凝集素,主要表達(dá)于肝細(xì)胞的竇狀表面�����。作為肝臟特異性受體�����,ASGPR的表達(dá)在HCC發(fā)生時(shí)顯著增強(qiáng)�。LA對(duì)ASGPR具有特異性,基于LA的PET探針和抗腫瘤藥物已被報(bào)道具有優(yōu)異的HCC特異性和腫瘤抑制作用�����。作者構(gòu)建了一個(gè)熒光LA衍生物(LABO),它具有粘度和濃度誘導(dǎo)的腫瘤內(nèi)原位自組裝的特征���,由于LA和ASGPR之間的識(shí)別����,LABO對(duì)HCC表現(xiàn)出很高的特異性�����。LABO在游離狀態(tài)下無熒光����,但在腫瘤中聚集時(shí)顯示近紅外熒光并產(chǎn)生輻照誘導(dǎo)的ROS,用于肝癌的近紅外成像和光動(dòng)力治療�。
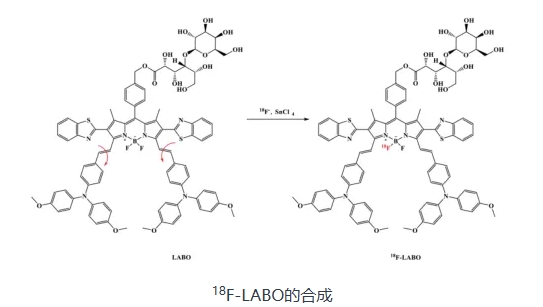
由于缺乏自組裝所需的黏度和藥劑濃度條件,再加上缺乏輻照����,為非靶器官提供了雙重安全保證。同時(shí)���,用18F標(biāo)記LABO通過18-19 F交換進(jìn)行PET成像時(shí)���,由于其結(jié)構(gòu)與LABO相似���,18F-LABO在腫瘤內(nèi)化前表現(xiàn)出一致的腫瘤特異性和體內(nèi)行為,可以提供腫瘤定位�����、分期和預(yù)后評(píng)價(jià)等詳細(xì)信息����。然而����,18F-LABO由于其極低的化學(xué)當(dāng)量而無法在腫瘤中進(jìn)行原位自組裝,這使得它在成像后能夠迅速?gòu)哪[瘤和代謝器官中清除�。

圖片來源:https://doi.org/10.1186/s12951-024-02879-6
近日,來自重慶醫(yī)科大學(xué)第一附屬醫(yī)院的研究者們?cè)?em>J Nanobiotechnology雜志上發(fā)表了題為“Construction of in-situ self-assembled agent for NIR/PET dual-modal imaging and photodynamic therapy for hepatocellular cancer”的文章���,該研究構(gòu)建了一種腫瘤內(nèi)原位自組裝劑(LABO)及其18F標(biāo)記PET探針(18F-LABO)���,可用于肝癌的熒光/PET雙模成像和光動(dòng)力治療。
肝細(xì)胞癌(HCC)仍然是一種危及生命的癌癥�,HCC成像和治療的藥物應(yīng)具有不同的瘤內(nèi)滯留時(shí)間��,構(gòu)建具有不同瘤內(nèi)滯留時(shí)間的藥物用于腫瘤成像或治療仍具有重要價(jià)值�。本研究構(gòu)建了一種靶向lasialglyprotein receptor (ASGPR)的乳酸衍生物(LABO)�,用于肝癌的熒光成像和光動(dòng)力治療。
圖片來源:https://doi.org/10.1186/s12951-024-02879-6
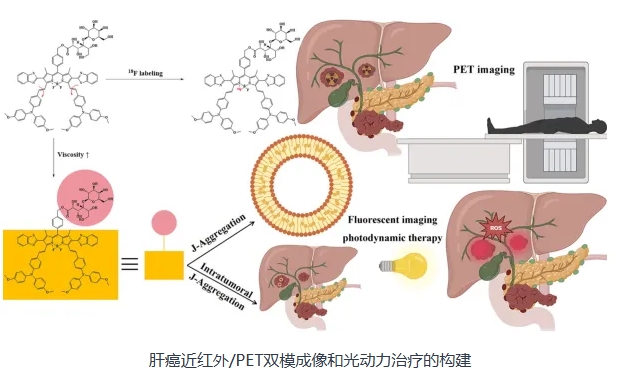
F標(biāo)記LABO (18F-LABO)用于肝細(xì)胞癌的PET成像����。LABO與18F-LABO分子結(jié)構(gòu)相似,LABO表現(xiàn)出黏性和濃度誘導(dǎo)的瘤內(nèi)自組裝特征��,擴(kuò)大了瘤內(nèi)潴留�����。LABO在游離期無熒光�,但自組裝后發(fā)出近紅外熒光并產(chǎn)生輻照誘導(dǎo)的ROS,用于熒光成像和光動(dòng)力治療����。用HepG2細(xì)胞證實(shí)LABO和18F-LABO對(duì)ASGPR的特異性。
生物分布和熒光成像證實(shí)了LABO和18F-LABO在用于光動(dòng)力治療和PET成像時(shí)的腫瘤保留時(shí)間不同��。對(duì)HepG2荷瘤小鼠進(jìn)行PET顯像和光動(dòng)力治療�,發(fā)現(xiàn)18F-LABO/LABO可在HepG2腫瘤中特異性積累,起到定位/抑制腫瘤的作用��。LABO/18F-LABO具有良好的HCC特異性,但其瘤內(nèi)行為不同�,在肝癌的PET/ NIR成像和光動(dòng)力治療中具有重要價(jià)值。
圖片來源:https://doi.org/10.1186/s12951-024-02879-6
綜上所述�����,本研究構(gòu)建了一種腫瘤內(nèi)原位自組裝劑(LABO)及其18F標(biāo)記PET探針(18F-LABO)�,用于肝癌的熒光/PET雙模成像和光動(dòng)力治療。LABO和18F-LABO具有良好的ASGPR特異性和合適的腫瘤內(nèi)行為����,具有作為HCC綜合治療工具的巨大潛力。(生物谷 Bioon.com)
轉(zhuǎn)載鏈接:https://news.bioon.com/article/d2868482100f.html
如有侵權(quán)請(qǐng)聯(lián)系我們�����,我們將會(huì)刪除�。
優(yōu)南推薦產(chǎn)品