人體內(nèi)源代謝化合物��,顧名思義�,就是人體內(nèi)產(chǎn)生和發(fā)現(xiàn)的一些代謝產(chǎn)物,這些代謝產(chǎn)物的作用可不容小覷����,不信我們就來看看它們有哪些作用:
一、內(nèi)源代謝產(chǎn)物可以用作疾病標(biāo)記物
疾病導(dǎo)致機(jī)體病理生理過程變化���,最終引起代謝產(chǎn)物發(fā)生相應(yīng)的改變�。代謝組學(xué)是繼基因組學(xué)和蛋白質(zhì)組學(xué)之后新發(fā)展起來的一門學(xué)科��,通過對某一生物或細(xì)胞中相對分子量小于1000的小分子代謝產(chǎn)物進(jìn)行定性和定量分析�����,尋找疾病的生物標(biāo)記物,將提供一種較好的疾病診斷方法�����。

比如在癌癥研究領(lǐng)域�,基于腫瘤細(xì)胞內(nèi)、外相關(guān)特征性小分子代謝標(biāo)記物的異常變化來診斷惡性腫瘤�、進(jìn)行藥物篩選、評價(jià)藥物毒性等的方法逐漸成為研究熱點(diǎn)�����。癌細(xì)胞具有一種獨(dú)特的�����、有別于正常細(xì)胞的代謝表型�,監(jiān)測癌細(xì)胞代謝過程中小分子代謝物的波動(dòng)情況,將有利于預(yù)測腫瘤的進(jìn)展���、了解體內(nèi)物質(zhì)代謝途徑�����、探索癌癥發(fā)病機(jī)制及藥物作用機(jī)制等�。目前的研究主要集中于與癌細(xì)胞能量代謝相關(guān)的化合物研究,如核苷類��、氨基酸類�����、脂類��、糖類等��。例如����,已發(fā)現(xiàn)多種與腫瘤相關(guān)的脂類標(biāo)記物����,膽堿、磷酸膽堿�、磷酸卵磷脂、膽固醇等脂類變化譜是細(xì)胞膜破壞的標(biāo)志�����;Pyruvic acid�����、乳酸、Isobutyric acid等是與腫瘤細(xì)胞糖代謝相關(guān)的生物標(biāo)記物��,探索通過靶向脂代謝��、糖代謝途徑治療惡性腫瘤的策略正備受關(guān)注�����。
二���、內(nèi)源代謝產(chǎn)物可用于藥物發(fā)現(xiàn)
除了用作疾病標(biāo)記物�,人體內(nèi)源性化合物本身還發(fā)揮著十分重要的生理作用����,并且大量研究結(jié)果證實(shí),許多疾病和內(nèi)源性物質(zhì)的異常改變密切相關(guān)����,因而,從研究內(nèi)源性活性物質(zhì)入手來尋找治療疾病的藥物�����,成為新藥研究最主要的途徑之一。并且��,以體內(nèi)生命基礎(chǔ)過程和生物活性物質(zhì)為基礎(chǔ)發(fā)現(xiàn)和基于體內(nèi)生物轉(zhuǎn)化的代謝產(chǎn)物而發(fā)現(xiàn)先導(dǎo)化合物也是先導(dǎo)化合物發(fā)現(xiàn)的主要途徑之一���。迄今已發(fā)現(xiàn)作為治療藥物靶點(diǎn)的總數(shù)約500個(gè)�,其中受體尤其是G-蛋白偶聯(lián)的受體(GPCR)靶點(diǎn)占絕大多數(shù)��,另還有酶��、抗菌�、抗病毒�����、抗寄生蟲藥的作用靶點(diǎn)�����。合理化藥物設(shè)計(jì)(rational drug design)可以依據(jù)生命科學(xué)研究中所揭示的包括酶�����、受體����、離子通道�����、核酸等潛在的藥物作用靶位�,或其內(nèi)源性配體以及天然底物的化學(xué)結(jié)構(gòu)特征來設(shè)計(jì)藥物分子�����,以發(fā)現(xiàn)選擇性作用于靶點(diǎn)的新藥��。

目前已有大量研究證實(shí)了部分人體內(nèi)源代謝產(chǎn)物的生物活性��。下面我們就來看一些例子:
1.含硫氨基酸代謝產(chǎn)物與心血管損傷和修復(fù)
哺乳動(dòng)物體內(nèi)存在以蛋氨酸作為起始的內(nèi)源性含硫氨基酸代謝途徑��,同型半胱氨酸(Hcy)����、胱硫醚和半胱氨酸為其重要中間代謝產(chǎn)物。?���;撬帷? hydrogen sulfide����,H2S) 和(sulfur dioxide�����,SO2) 等為其代謝終末產(chǎn)物����。這些同一代謝來源的活性分子具有各自相對獨(dú)立的生物學(xué)效應(yīng)���,但又彼此相互作用��,形成具有網(wǎng)絡(luò)調(diào)節(jié)關(guān)系的含硫氨基酸代謝分子群�����,是生物穩(wěn)態(tài)調(diào)節(jié)的重要物質(zhì),在心血管損傷和修復(fù)過程中發(fā)揮重要調(diào)控作用�。
同型半胱氨酸(Hcy)是多功能損傷因子,會損傷細(xì)胞結(jié)構(gòu)和功能����;內(nèi)源性H2S是機(jī)體重要的心血管防御體系,具有廣泛的心血管系統(tǒng)調(diào)節(jié)作用���;?�;撬峋哂修卓箘?dòng)脈粥樣硬化���、高血壓和胰島素抵抗等效應(yīng)�����,是一個(gè)廣譜的心血管細(xì)胞保護(hù)劑�����。
2.犬尿氨酸代謝途徑異常與中樞神經(jīng)系統(tǒng)疾病修復(fù)
犬尿氨酸代謝途徑(kynurenine pathway�����,KP) 是腦內(nèi)色氨酸代謝的重要通路��。近些年研究發(fā)現(xiàn)�,多種中樞神經(jīng)系統(tǒng)疾病的理化改變與該通路代謝紊亂相關(guān)����。KP主要功能是促進(jìn)糖酵解、抑制糖異生,為腦組織提供必要的物質(zhì)能量支持��,對炎癥刺激和細(xì)胞毒性作用下神經(jīng)元的保護(hù)尤為重要�。另外,KP中部分衍生物�,可影響腦內(nèi)神經(jīng)遞質(zhì)的含量和功能,對中樞神經(jīng)系統(tǒng)疾病的發(fā)生和調(diào)控具有重要意義���。
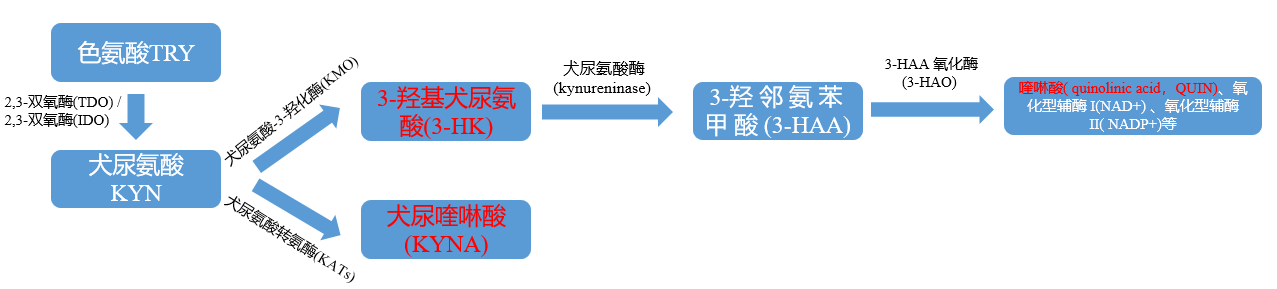
色氨酸TRY經(jīng)色氨酸2���,3-雙氧酶(TDO) 或吲哚胺2,3-雙氧酶 (IDO) 分解生成犬尿氨酸KYN�����。KYN 進(jìn)一步分解通過以下兩途徑:(1)經(jīng)犬尿氨酸-3-羥化酶(KMO)催化生成3-羥基犬尿氨酸(3-HK) ����,再由犬尿氨酸酶(kynureninase) 催化生成(3-hydroxyanthranilic acid,3-HAA)�,最終由3-HAA氧化酶( 3-HAO)分解為(quinolinic acid���,QUIN)�,氧化型輔酶I(NAD+) �、氧化型輔酶II(NADP+)等;(2)在犬尿氨酸轉(zhuǎn)氨酶(kynurenine aminotransferas-es�,KATs) 作用下生成 (kynurenic acid�,KYNA) 。
KYNA是一種廣譜的促離子型谷氨酸鹽受體拮抗劑���,特定作用于N-甲基-D-天冬氨酸 (N-methyl-D-aspartate�,NMDA)受體上的甘氨酸結(jié)合位點(diǎn)����,可抑制谷氨酸遞質(zhì)過度興奮性傳遞,同時(shí)能拮抗(α7-nAChR)�,降低神經(jīng)細(xì)胞外谷氨酸(Glu)和多巴胺(DA)水平。與KYNA作用截然相反�����,QUIN為NMDA受體激動(dòng)劑���,腦內(nèi) QUIN 增多可激活 NMDA 受體����,誘發(fā)興奮性毒性作用�。3-HK可引起神經(jīng)細(xì)胞凋亡,而QUIN 可引起神經(jīng)細(xì)胞退行性改變。KYNA可對抗QUIN 起到神經(jīng)保護(hù)作用��,盡管如此��,作為一種廣泛的離子型興奮性氨基酸受體拮抗劑�����,當(dāng)KYNA過度積累超過正常水平時(shí)���,將削弱谷氨酸能遞質(zhì)的生物功能����,導(dǎo)致認(rèn)知功能紊亂����。
3.人體內(nèi)源小分子促進(jìn)腫瘤干細(xì)胞分化,阻止腫瘤增殖
2015年6月10日����,浙江大學(xué)醫(yī)學(xué)院附屬醫(yī)院王英杰教授課題組在《自然通訊》(Nature Communications)上發(fā)表了題為“Tryptophan derivatives regulate the transcription of Oct4 in stem-like cancer cells”的研究論文,揭示色氨酸的一種代謝產(chǎn)物ITE可以促進(jìn)腫瘤干細(xì)胞的分化�����。研究人員發(fā)現(xiàn)��,在腦膠質(zhì)瘤���、肝癌等腫瘤細(xì)胞中�����,內(nèi)源產(chǎn)生的色氨酸代謝物ITE [2-(1’H3’-吲哚羰基)噻唑-4-羧酸甲酯]可作為配體激活一類稱為芳香烴受體(AhR)的核轉(zhuǎn)錄因子���,促使AhR結(jié)合在核心干性因子Oct4基因的啟動(dòng)子區(qū),抑制Oct4轉(zhuǎn)錄��。當(dāng)腫瘤微環(huán)境中色氨酸等氨基酸耗竭或局部缺氧等條件導(dǎo)致ITE濃度下降時(shí)���,原先結(jié)合的AhR會脫離Oct4啟動(dòng)子�����,使Oct4表達(dá)上調(diào)���,啟動(dòng)腫瘤干細(xì)胞形成。加入化學(xué)合成的外源ITE后����,Oct4表達(dá)上調(diào)被有效抑制和逆轉(zhuǎn)�����,腫瘤干細(xì)胞發(fā)生分化�。把腫瘤細(xì)胞異位或原位接種至裸鼠形成移植瘤后���,ITE腹腔注射或瘤內(nèi)注射均能顯著抑制瘤體增殖�����。
由上述案例可以看出人體內(nèi)源代謝產(chǎn)物發(fā)揮著極為重要的生理作用���,而且近年來,有研究人員提出藥物的“代謝產(chǎn)物類似性(metabolite-likeness)”可作為篩選藥物的評價(jià)指標(biāo)之一�。有研究評價(jià)了已上市藥物和藥物篩選化合物庫與內(nèi)源代謝物的類似性,發(fā)現(xiàn)已上市藥物和內(nèi)源代謝物更為類似�,可能的機(jī)制有兩方面:一方面,大多數(shù)藥物進(jìn)入細(xì)胞需要溶質(zhì)載體的協(xié)助�,這些溶質(zhì)載體在體內(nèi)用于轉(zhuǎn)運(yùn)內(nèi)源代謝產(chǎn)物,而與內(nèi)源代謝產(chǎn)物類似的藥物更容易與這些溶質(zhì)載體結(jié)合從而進(jìn)入細(xì)胞����;另一方面��,藥物可能以與天然底物類似的方式與其靶點(diǎn)進(jìn)行結(jié)合����,故藥物和內(nèi)源代謝產(chǎn)物有更高的類似性���。
看到這里小編不禁要驚呼,原來自己的身體就是一個(gè)巨大的藥物寶庫啊�����,那不是又讓藥物篩選多了一線曙光嗎��?但是你可能要問���,人體內(nèi)這么多內(nèi)源代謝產(chǎn)物����,恐怕收集起來也很費(fèi)勁吧�����?不用擔(dān)心�,TargetMol已經(jīng)替你收集了665種內(nèi)源代謝產(chǎn)物�,組成人內(nèi)源代謝化合物庫��,是探索疾病發(fā)病機(jī)制和尋找新藥的有效工具�。
安全可靠:是源自體內(nèi)的代謝產(chǎn)物,安全性得以保障�����;且部分已經(jīng)上市或進(jìn)入臨床����;
種類多樣:包括羧酸、氨基酸����;生物胺、多胺��;核苷酸�、輔酶和維生素;單糖和雙糖�����;脂肪酸�����、脂類、類固醇和激素等不同種類代謝相關(guān)產(chǎn)物����;
信息詳細(xì):化合物分子式、分子量���、SMILES、產(chǎn)品描述����、化合物種類、細(xì)胞分布����、生物樣本分布、組織分布���、相關(guān)疾病及參考文獻(xiàn)等�;
品質(zhì)保證:NMR�����、HPLC/LCMS等多種檢測技術(shù)保證產(chǎn)品結(jié)構(gòu)正確,純度高�����,減少假陽性����。
目前這個(gè)化合物庫已經(jīng)服務(wù)于細(xì)胞誘導(dǎo)、抗腫瘤研究�、抗病毒研究、代謝疾病研究等方向的科研用戶�����,如果你也對這個(gè)化合物庫感興趣或有任何疑問��,歡迎撥打400-821-2233或發(fā)送郵件至info@tsbiochem.com咨詢哦~
參考文獻(xiàn):
- Barroso M�����,Rocha MS�,Esse R,et al. Cellular hypomethylation is associated with impaired nitric oxide production by cultured human endothelial cells.Amino Acids�,2011,42: 1903~1911.
- Guillemin GJ. Quinolinic acid, the inescapable neurotoxin. FEBS J,2012�����,279: 356~1365.
- Cheng J, Li W, Kang B, et al. Tryptophan derivatives regulate the transcription of Oct4 in stem-like cancer cells[J]. Nature Communications, 2015, 6:7209.
- Gupta S, Aires-De-Sousa J. Comparing the chemical spaces of metabolites and available chemicals: models of metabolite-likeness. Molecular Diversity, 2007, 11(1):23-36.
- Dobson PD, Patel Y, Kell DB. Metabolite-likeness" as a criterion in the design and selection of pharmaceutical drug libraries. Drug Discovery Today, 2009, 14(1–2):31–40.
- O’Hagan S, Swainston N, Handl J, Kell DB. A ‘rule of 0.5′ for the metabolite-likeness of approved pharmaceutical drugs. Metabolomics, 2015, 11(2):323–339
- O’Hagan S, Kell DB. Understanding the foundations of the structural similarities between marketed drugs and endogenous human metabolites. Front Pharmacol, 2015, 6:105
- O’Hagan S, Kell DB. MetMaxStruct: a Tversky-similarity-based strategy for analysing the (sub)structural similarities of drugs and endogenous metabolites. Front Pharmacol, 2016, 7:266