Wei-Phos配體(以周偉博士名字命名的配體)是張俊良教授課題組基于非C2對稱性���、剛?cè)岵图婢哕浻才湮辉?O, S, N, P原子)的設(shè)計理念�,開發(fā)的第一例雙膦Sadphos(Sulfinamide Phosphine的簡稱)配體。該配體從商業(yè)可得2-二芳基膦芳基甲醛出發(fā)�,與叔丁基亞磺酰胺縮合制備亞胺,之后與二苯基膦亞甲基鋰進行加成�����,經(jīng)過兩步反應(yīng)即可通過柱層析或重結(jié)晶方便獲得(圖1)[1]��。目前�����,Wei-Phos在手性膦催化���、手性高分子材料合成和不對稱金屬催化領(lǐng)域表現(xiàn)出優(yōu)異的催化活性和手性誘導(dǎo)能力(圖 1)。下面���,將按照反應(yīng)類型對Wei-Phos配體在不對稱轉(zhuǎn)化中的應(yīng)用進展做簡要介紹�。

圖1. Wei-Phos 的合成及應(yīng)用
叔膦催化是有機催化的重要組成部分����,近幾十年來,以Morita-Baylis-Hillman反應(yīng)����、Rauhut–Currier反應(yīng)和陸氏[3+2]環(huán)加成等為代表的叔膦催化反應(yīng)已經(jīng)成為構(gòu)建官能化有機分子的重要合成手段�����,部分轉(zhuǎn)化已成功應(yīng)用于天然產(chǎn)物的合成中���。在叔膦催化領(lǐng)域,新型高效手性膦催化劑的開發(fā)一直備受化學(xué)家廣泛關(guān)注�����,具有很大挑戰(zhàn)性�����。針對這一難題��,張俊良教授課題組從商業(yè)可得2-二芳基膦芳基甲醛出發(fā)���,與叔丁基亞磺酰胺縮合制備亞胺�����,之后與二苯基膦亞甲基鋰進行加成�����,簡潔高效構(gòu)建了一系列β-氨基手性雙膦催化劑(Wei-Phos)并考察了其應(yīng)用��。
Rauhut–Currier反應(yīng)是一個高效構(gòu)筑碳-碳鍵的基礎(chǔ)反應(yīng)����,具有高原子經(jīng)濟性、產(chǎn)物含多種官能團的優(yōu)點���。自該反應(yīng)被發(fā)現(xiàn)以來�����,一直存在著局限性���,如不同烯烴的交叉反應(yīng)沒有選擇性,催化劑用量大�����,反應(yīng)底物范圍不廣���。張俊良教授課題組針對Rauhut–Currier反應(yīng)的缺點�,通過新催化劑的開發(fā)����,成功實現(xiàn)了不同活潑烯烴間的不對稱交叉Rauhut–Currier反應(yīng)(圖2)。機理研究表明���,在反應(yīng)過程中Wei-Phos中的兩個叔膦單元各司其職:二苯基亞甲基膦部分電子云密度較高�����,在反應(yīng)過程中起到親核加成的催化作用���;三芳基膦部分電子云密度較低,在反應(yīng)過程中扮演剛性位阻的作用���。

圖2. Wei-Phos 在不對稱分子間Rauhut–Currier反應(yīng)中的應(yīng)用
2018年���,張俊良教授課題組對Wei-Phos進行了進一步修飾。Wei-Phos中叔丁基亞磺?�;糠衷谒嵝詶l件下可以被脫除��,進而引入酰胺或與氨基酸縮合得到具有更強氫鍵供體能力的催化劑。隨后張俊良教授將這類新修飾的催化劑應(yīng)用于鄰亞甲基苯醌 (o-QMs)與MBH碳酸酯的[4+1]環(huán)加成反應(yīng)中��,取得了優(yōu)異的對映選擇性(圖3)

圖3. Wei-Phos 催化o-QMs與MBH碳酸酯不對稱 [4+1]環(huán)加成反應(yīng)
同年����,華東理工大學(xué)李浩教授課題組也利用修飾后的Wei-Phos實現(xiàn)了2-烯基吡啶與活潑烯烴間的不對稱Rauhut–Currier反應(yīng),取得了良好的產(chǎn)率和優(yōu)異的對映選擇性(圖4)[3]�。李浩教授課題組的這一研究工作進一步拓展了 Rauhut–Currier反應(yīng)的底物范圍,為官能化的手性吡啶化合物的構(gòu)建提供了一種新的途徑��。

圖4. Wei-Phos 催化2-烯基吡啶與活潑烯烴不對稱分子間Rauhut–Currier反應(yīng)
手性聚合物是一類特殊的高分子材料����,具有區(qū)別于傳統(tǒng)高分子材料的特殊性質(zhì),比如空間排布�����、材料強度����、介電性能以及可塑性等方面。而這些特殊的性質(zhì)賦予了手性聚合物獨特的功能和應(yīng)用�����,如手性分離材料�、手性液晶材料、手性傳感材料和手性電磁材料等��。因此��,手性聚合物材料的合成具有重要的科學(xué)意義和市場價值�����。手性催化劑誘導(dǎo)非手性單體的立體選擇性聚合是構(gòu)建手性高分子材料的重要途徑之一���。近年來Wei-Phos在不對稱高分子聚合領(lǐng)域的應(yīng)用越來越廣泛���,在多種聚合反應(yīng)中表現(xiàn)出了優(yōu)異的催化活性和手性誘導(dǎo)能力。
高分子端基功能化是指在高分子聚合物的端基上引入新的功能基團��,賦予其性質(zhì)和功能�����,是高分子功能化的重要手段��。2018年��,合肥工業(yè)大學(xué)吳宗銓教授課題組利用鈀/Wei-Phos催化體系實現(xiàn)了螺旋聚卡賓的高效活性可控合成,制備出了一種結(jié)構(gòu)新穎的螺旋高分子(圖5)����。
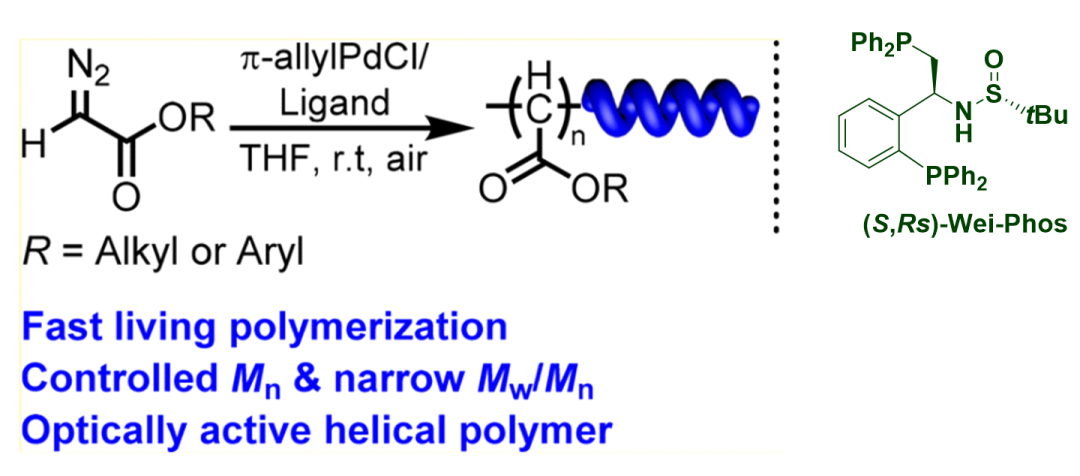 圖5. Wei-Phos 在合成螺旋聚卡賓中的應(yīng)用
圖5. Wei-Phos 在合成螺旋聚卡賓中的應(yīng)用
環(huán)丙烯類(CPEs)是最小的不飽和環(huán)狀化合物,它們因極高的環(huán)張力而表現(xiàn)出豐富的反應(yīng)性����,被廣泛應(yīng)用在有機合成和開環(huán)易位聚合(ROMP)方面,但是環(huán)丙烯中乙烯基的加聚反應(yīng)研究報道較少�����,相關(guān)的活性/可控聚合仍是一個極大的難題�,主要的難點在于聚合過程中的動力學(xué)障礙和中間體的內(nèi)在不穩(wěn)定性。2021年����,北京大學(xué)王劍波教授團隊以[Pd(allyl)Cl]2為Pd源、Wei-Phos為配體����,成功報道了一例催化環(huán)丙烯類化合物的活性/可控乙烯基加聚反應(yīng)[9],通過該反應(yīng)可以得到包含完全飽和的剛性三元環(huán)結(jié)構(gòu)的主鏈聚合物(圖7)�,產(chǎn)率中等偏上,并且具有可控的Mn和較小的Mw/Mn值��。
 圖7. Wei-Phos 在環(huán)丙烯聚合中的應(yīng)用
圖7. Wei-Phos 在環(huán)丙烯聚合中的應(yīng)用
三、不對稱金屬催化
可見光催化作為一種綠色�、可持續(xù)的新興策略,被廣泛用于有機合成領(lǐng)域�。有機化學(xué)家結(jié)合不對稱有機催化��、過渡金屬催化�����、酶催化等立體控制策略發(fā)展了有效的不對稱可見光催化策略�。盡管近幾年該領(lǐng)域得到了快速的發(fā)展,但主要用于中心手性化合物合成��。近日���,華中師范大學(xué)的肖文精��、陸良秋團隊報道了首例可見光誘導(dǎo)的不對稱鈷/Wei-Phos協(xié)同催化自由基偶聯(lián)反應(yīng)����,實現(xiàn)了外消旋聯(lián)雜芳基化合物動態(tài)動力學(xué)不對稱轉(zhuǎn)化(圖8)�����。該反應(yīng)成功的關(guān)鍵在于氧化加成后形成的軸手性芳基鈷物種由于吡啶的配位作用,減小了旋轉(zhuǎn)能壘和消旋化����,隨后立體選擇性地捕獲光催化產(chǎn)生的自由基。

圖8. Wei-Phos 在光催化自由基不對稱偶聯(lián)中的應(yīng)用
近日��,肖文精教授課題組進一步研究了光誘導(dǎo)鈷催化動態(tài)動力學(xué)還原共軛加成反應(yīng)����,Wei-Phos在上述反應(yīng)中依然保持了優(yōu)異的催化活性和手性誘導(dǎo)能力(圖9)?����;谏鲜霾呗?����,肖文精教授與合作者成功合成了一系列具有軸手性的雜二芳基衍生物(45個實例��,收率高達91%�,ee高達97%)。該反應(yīng)具有反應(yīng)條件溫和��、官能團耐受性良好���、對映選擇性出色等特點��。值得注意的是�����,該條件可避免大量金屬廢物的生成以及貴金屬催化劑的使用���。

圖9. Wei-Phos 在光催化自由基不對稱加成中的應(yīng)用
相關(guān)產(chǎn)品推薦
凱若利專注于研發(fā)各類手性催化劑,手性技術(shù)相關(guān)的技術(shù)開發(fā),技術(shù)轉(zhuǎn)讓��。能夠提供各類手性NHC配體���,質(zhì)量可靠穩(wěn)定�,能夠供應(yīng)從毫克級到公斤級的產(chǎn)品���。以下是部分手性NHC配體�����,更多系列產(chǎn)品請詳詢�����。
